Fágová terapie
Mikroorganismy jsou všude kolem nás, na našem těle i uvnitř něj. Věděli jste, že se v lidském těle nachází více bakterií než lidských buněk? Je těžké najít některou oblast našich životů, která není mikroorganismy ovlivněna. Jsou v našem zažívacím systému, jiné způsobují nemoci, další se používají při výrobě potravin (například sýrů, piva nebo kysaného zelí) nebo napomáhají rozkladu kompostu, který se používá ke hnojení při pěstování plodin. Až takto jsou významné.
Stále tíživější situací pro lidstvo jsou rostoucí počty a šíření mikroorganismů odolných vůči antibiotikům. Tyto bakterie nereagují na léčbu antibiotiky, což je opravdu velký problém hlavně u těch, které způsobují potenciálně smrtelná onemocnění. Bez antibiotik se vrátíme do dob, kdy byly situace jako pořezaný prst, porod dítěte nebo operace životu nebezpečné kvůli riziku vzniku infekce. V současné době, která je předehrou „antibiotikové apokalypsy“, začal závod s časem o to, najít nové cesty pro boj s patogenními mikroorganismy, nová antibiotika a lépe porozumět tomu, jak vlastně patogenní mikroorganismy fungují.
Na konci roku 2018 byla po třiceti letech objevena nová třída antibiotik, což je skvělá zpráva, ale i přesto se stále snažíme vyvinout další nástroje, jež nám pomohou se s bakteriální rezistencí vyrovnat. Existuje spousta směrů, kterými se vědci vydávají. V České republice skupina Pavla Plevky ze Středoevropského technologického institutu (CEITEC) na Masarykově univerzitě využívá pro výzkum kryogenní mikroskopy CEITECu spolu se superpočítačem IT4Innovations národního superpočítačového centra.

Elektronový mikroskop Titan Krios umožňuje zobrazení makromolekul a buněk v tzv. vitrifikovaném stavu (vzorek je zamražen do velmi tenké vrstvy ledu).
Již od počátků mikrobiologie, kdy holandský vědec Antonie van Leeuwenhouk popsal existenci miniaturních organismů, které nazval „animalcules“, byla klíčovou technikou jejich zkoumání právě mikroskopie. Obrázky se původně překreslovaly ručně, poté byl používán fotografický film, nyní už jsou běžné digitální snímky. Obrázků bakteriofágů je třeba vyfotit velké množství, a proto zabírají významnou část počítačové paměti a pro analýzu vyžadují silný výkon procesorů. Chceme-li studovat tato stále komplexnější obrazová data, je využití superpočítačů – i z pohledu pokroku v dané oblasti výzkumu – nezbytné.
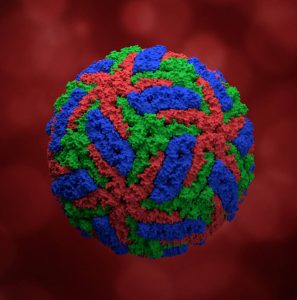
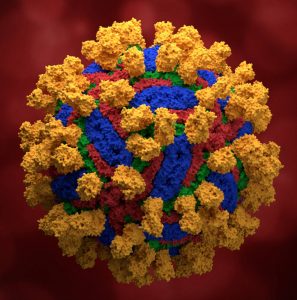
Pavel Plevka a jeho kolegové využili tyto nejmodernější technologie a zdroje pro určení struktury několika druhů organismů – pikornavirů – odpovědných za nemoci, jako jsou běžné nachlazení, slintavka a kulhavka nebo encefalitida; dále virů, které způsobují úbytek včelstev v USA i Evropě; flavivirů – zejména encefalitidy přenášené klíšťaty (TBEV), jež zapříčiňuje mnoho úmrtí v České republice i ve světě; a leishmaniózy, která způsobuje vředy na lidské kůži.
Zvláštní pozornost věnuje tato výzkumná skupina bakteriofágům, což jsou viry, které umí nakazit a zničit bakteriální buňky. Velmi slibnou se zdá být možnost využití bakteriofágů k eliminaci infekce zlatého stafylokoka (Staphylococcus aureus). Zlatý stafylokok je široce rozšířený, potenciálně patogenní a vůči antibiotikům stále více odolný druh bakterie, který trápí pacienty nemocnic po celém světě. Tato bakterie může způsobit život ohrožující infekce zejména lidem, jejichž organismus je už oslaben jinou nemocí. Bez technologického pokroku v mikroskopii a využití superpočítačů by rozvoj fágové terapie nebyl možný.
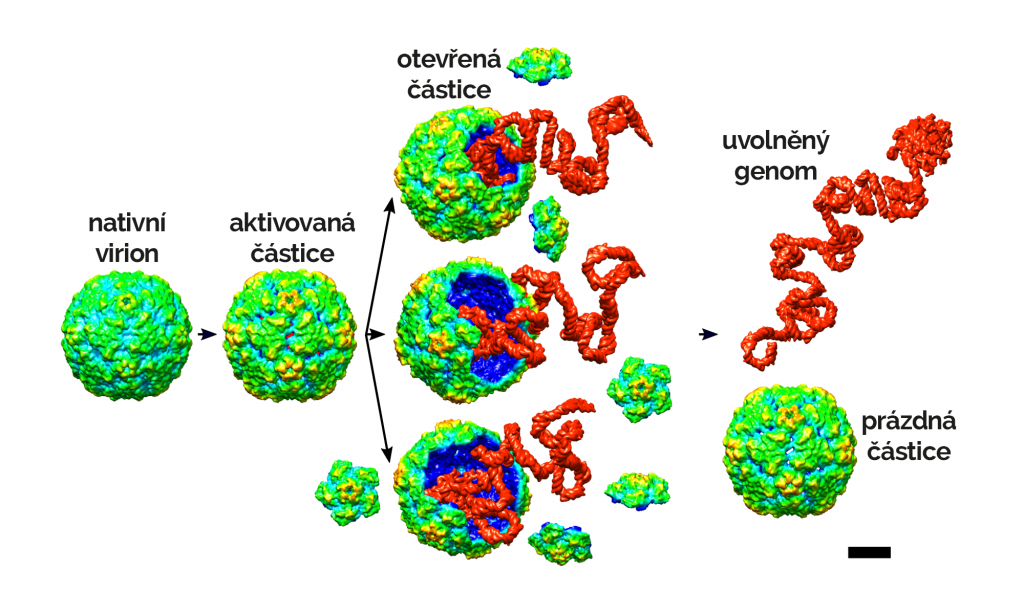
Uvolnění genomu enteroviru. Při vystavení enterovirů kyselému pH dochází ke konformační změně viru v aktivovanou částici. Strukturní změny v obalu virové částice a genomu umožní vyloučení pentamerů z obalu viru, čímž dojde k jeho otevření. Šroubovice RNA je z takto otevřené částice uvolněna. Měřítko představuje 10 nm.
Více o práci Pavla Plevky na: http://plevkalab.ceitec.cz