Mutacje genetyczne a choroba Alzheimera
Nazwa projektu: FEHERJEK; Lider projektu: Gábor Paragi
Instytucja macierzysta: MTA-SZTE Biomimetic Systems Research Group, Węgierska Akademia Nauk – Uniwersytet w Szeged, Szeged, Węgry i Instytut Fizyki, Uniwersytet w Pecs, Pecs, Węgry
Choroba Alzheimera atakuje mózg, prowadząc do stopniowej utraty pamięci i innych ważnych funkcji poznawczych. Chociaż choroba nie jest dziedziczna, istnieją czynniki genetyczne, które mogą zwiększyć prawdopodobieństwo jej rozwoju. Do obecnej dekady powszechnie uważano, że demencja związana z tą chorobą była wynikiem akumulacji peptydu amyloidowego β (budulca białka, cząsteczki tworzącej mięso) w mózgu, tworząc struktury zwane płytkami. A uważano tak, ponieważ płytki te znaleziono w mózgu każdego pacjenta, który zmarł na Alzheimera. Obecnie jednak staje się oczywiste, że za uszkodzenia neuronów w mózgu mogą być odpowiedzialne inne toksyczne postacie tych peptydów Aβ (oligomery peptydu Aβ).
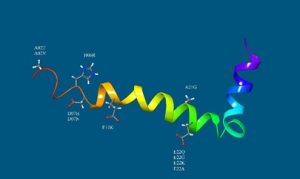
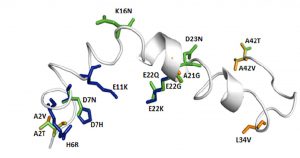
Na Węgrzech, Gábor Paragi wraz ze swoimi współpracownikami z MTA-SZTE Biomimetic Systems Research Group (Węgierska Akademia Nauk na Uniwersytecie w Szeged) i Instytutu Fizyki (na Uniwersytecie w Pecs) badają procesy prowadzące do powstawania płytki, poszukując wskazówek i przyczyn choroby Alzheimera. W wieluwcześniejszych badaniach pomijano działanie peptydów Aβ ponieważ najdokładniej badano produkty końcowe, czyli płytki, które uważano za krytyczne.badano . Jednak podczas badania procesu powstawania peptydów Aβ Gábor Paragi i jego zespół zrozumieli, że mutacje w składnikach (monomerach), które tworzą peptydy Aβ, mogą prowadzić do efektów toksycznych.
Grupa badawcza wykorzystuje techniki Wymiany repliki w dynamice molekularnej (ang. Replica Exchange Molecular Dynamics), korzystając z zasobów obliczeniowych i mocy Rządowej Agencji Rozwoju Technologii Informacyjnych do analizowania dynamiki molekularnej w trakcie tego procesu. Odkryto powiązania między obecnością pewnej struktury a zmutowanymi toksycznymi peptydami. Odkrycie to z pewnością przyczyni się do lepszego zrozumienia mechanizmów choroby Alzheimera i większej efektywności leczenia cierpiących pacjentów i ich ich rodzin na całym świecie.
Szczególne podziękowania kierujemy do Rządowej Agencji Rozwoju Technologii Informacyjnych za udostępnienie zasobów obliczeniowych na klastrze Debrecen2 (Leo) GPU. Prace te były wspierane przez rząd węgierski, numer grantu GINOP-2.3.2-15-2016-00034 oraz GINOP-2.3.2-15-2016-00032.